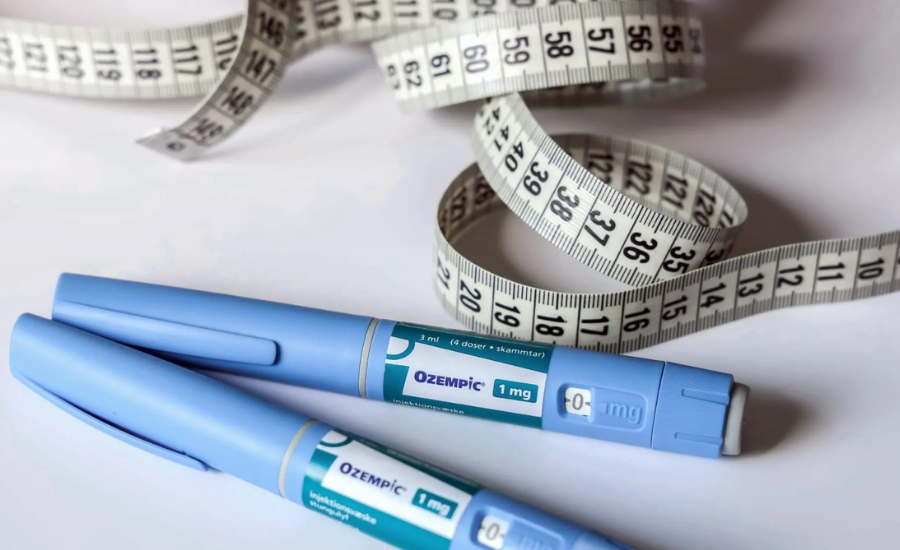
A patente da semaglutida, substância utilizada em medicamentos como o Ozempic, expira nesta sexta-feira (20) no Brasil. Com o fim da proteção, abre-se a possibilidade de entrada de novos produtos no mercado, o que pode ampliar a oferta e reduzir os preços.
Segundo dados da Agência Nacional de Vigilância Sanitária (Anvisa), atualmente há oito processos em análise relacionados a medicamentos com o mesmo princípio ativo. Entre eles, dois pedidos de registro de semaglutida sintética estão em fase de exigência, dependendo do envio de informações adicionais pelas empresas para continuidade da avaliação.
“Nos dois casos, o prazo para resposta das empresas é até o final de junho e, por isso, não é possível definir prazos para conclusão do processo. Na área de biológicos, um produto está em análise e outro aguarda início de avaliação”, informou a agência.
De acordo com a Anvisa, os demais pedidos em análise devem receber posicionamento técnico até o fim de abril. “Esta posição pode ser pela aprovação, reprovação ou apresentação de exigência técnica”.
Diferenças entre os produtos
Os medicamentos à base de semaglutida atualmente disponíveis no país são classificados como biológicos. Já os novos pedidos em avaliação incluem tanto produtos biossimilares, obtidos por via biológica, quanto versões sintéticas, produzidas por síntese química.
A agência destaca que, no caso de medicamentos biológicos, não há possibilidade de registro como genéricos. “No caso de medicamentos biológicos, não existe a opção de registro como genéricos, por isso, o produto deve se enquadrar em uma das duas categorias citadas acima. Esses produtos podem ser avaliados a partir de diversos ensaios de comparação com o produto biológico, mas não são genéricos nem similares – são análogos sintéticos de produtos biológicos.”
Desafios regulatórios
A avaliação de versões sintéticas da semaglutida tem sido apontada como um desafio técnico para agências reguladoras em diferentes países. Até o momento, segundo a Anvisa, nenhuma das principais autoridades sanitárias internacionais aprovou esse tipo de produto.
“Até o momento, nenhuma das principais agências de medicamentos do mundo, como as do Japão, Europa e Estados Unidos, registrou análogos sintéticos da semaglutida”.
Ainda segundo a agência, a análise desses medicamentos exige critérios que combinam parâmetros aplicados a fármacos sintéticos e biológicos.
“Um dos motivos é a necessidade de avaliar estes produtos utilizando parâmetros tanto de fármacos sintéticos como de biológicos. Isso ocorre porque esses produtos compartilham preocupações típicas de medicamentos sintéticos (ex. resíduos de solventes no processo, resíduos de catalisadores metálicos, impurezas com estrutura química semelhante) quanto as de produtos biológicos (ex. Risco de imunogenicidade, formação de agregados, entre outros).”
Entre os principais pontos avaliados estão a presença de impurezas, a formação de agregados, a esterilidade e o potencial de provocar respostas imunológicas.
“A avaliação busca garantir, por exemplo, que o medicamento não provoque reações imunes indesejadas, como a criação de anticorpos anti-fármaco, que podem levar à ineficácia de qualquer semaglutida para o paciente, ou mesmo reações de imunidade mais graves.”
Decisão judicial
Em janeiro, a Quarta Turma do Superior Tribunal de Justiça (STJ) decidiu não prorrogar o prazo de vigência das patentes do Ozempic e do Rybelsus, outro medicamento que utiliza a semaglutida, mas em formato oral.
A ação foi movida pela Novo Nordisk e pela Novo Nordisk Farmacêutica do Brasil Ltda., que solicitaram o reconhecimento de demora administrativa na análise das patentes pelo Instituto Nacional da Propriedade Industrial (Inpi).
As instâncias anteriores negaram o pedido, com base no entendimento consolidado após o julgamento da Ação Direta de Inconstitucionalidade 5.529 pelo Supremo Tribunal Federal (STF), que fixa em 20 anos o prazo de vigência de patentes a partir do depósito, sem possibilidade de extensão judicial.